Хиральность (химия)
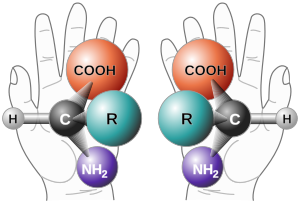
Хиральность (др.-греч. χείρ «рука») — свойство молекулы не совмещаться в пространстве со своим зеркальным отражением[1]. Термин основан на древнегреческом названии наиболее узнаваемого хирального предмета — руки. Так, левая и правая руки являются зеркальными отражениями, но не могут быть совмещены друг с другом в пространстве. Подобным образом, свойством хиральности обладают молекулы, в которых отсутствуют зеркально-поворотные оси симметрии Sn, что эквивалентно наличию в молекуле элементов хиральности: центра, оси, плоскости хиральности и др. Такие зеркально-симметричные формы химических соединений называются энантиомерами.
История[править | править код]

Хиральность молекул была открыта Л. Пастером в 1848 году. Пастер обратил внимание на то, что кристаллы, выпадающие из раствора рацемического тартрата натрия-аммония, имеют две формы, представляющие собой зеркальные отражения, которые не совмещаются друг с другом в пространстве. Напротив, кристаллы индивидуального правовращающего тартрата натрия-аммония имели одинаковую форму с малыми плоскостями, направленными в одну сторону. Пастер провёл подобные кристаллизации с тринадцатью энантиомерно чистыми соединениями (различными тартратами и винной кислотой), а также с шестью рацемическими тартратами и сделал вывод о существовании хиральности молекул и объяснил ранее неизвестный вид изомерии винных кислот — энантиомерию[2].
Структурная трактовка хиральности стала возможной после введения в 1874 году Я. Вант-Гоффом и Ж. Ле Белем концепции асимметрического атома углерода, то есть тетраэдрического атома углерода с четырьмя различными заместителями[2].
Понятие хиральности было введено лордом Кельвином в конце XIX в.[3][4]
Я называю какую-либо геометрическую фигуру, или группу точек, хиральной и говорю, что она обладает хиральностью, если её изображение в идеальном плоском зеркале не может быть с ней совмещено.
Оригинальный текст (англ.)I call any geometrical figure, or group of points, chiral, and say it has chirality, if its image in a plane mirror, ideally realized, cannot be brought to coincide with itself.— У. Т. Кельвин. Балтиморские лекции по молекулярной динамике и волновой теории света, 1904
Позже В. Мейер распространил понятие о хиральности на соединения азота, а У. Дж. Поуп — на атомы серы, селена и олова. Хиральность комплексных соединений металлов была изучена А. Вернером[5] .
Симметрия хиральных молекул[править | править код]
Поскольку хиральность является геометрической характеристикой, её можно определить путём отнесения молекулы к той или иной группе симметрии. Очевидно, не являются хиральными молекулы с центром инверсии (i) или плоскостью симметрии (s), поскольку эти молекулы состоят из двух одинаковых частей, которые при отражении превращаются друг в друга, и отражение является эквивалентным исходной молекуле. Ранее геометрический критерий хиральности формулировали так: «у хиральной молекулы не должно быть плоскости симметрии и центра инверсии». В настоящее время пользуются более точным критерием, который предполагает отсутствие у хиральной молекулы также зеркально-поворотных осей Sn[1][6].
Виды хиральности[править | править код]

В зависимости от элемента молекулы, наличие которого приводит к возникновению хиральности, различают следующие виды хиральности:
- центральная (центр хиральности)
- аксиальная (ось хиральности)
- планарная (плоскость хиральности)
- спиральная (спираль)
- топологическая.[6][7]
Центральная хиральность[править | править код]
Центральная хиральность возникает в результате наличия в молекуле центра хиральности (хирального центра), которым, как правило, является асимметрический атом углерода, имеющий 4 различных заместителя. Хиральными центрами могут быть также атомы Si, P, S, реже — N[8]. В хиральных производных адамантана центр хиральности находится в середине углеродного каркаса, где атомов нет вовсе[6].
Аксиальная (осевая) хиральность[править | править код]
Аксиальная хиральность возникает в результате неплоского расположения заместителей относительно некоторой оси — оси хиральности[9]. Ось хиральности существует в несимметрично замещённых алленах. sp-гибридный атом углерода в аллене имеет две взаимно перпендикулярные p-орбитали. Их перекрывание с p-орбиталями соседних атомов углерода приводит к тому, что заместители в аллене лежат во взаимно перпендикулярных плоскостях. Подобная ситуация наблюдается также в замещённых бифенилах, в которых вращение вокруг связи, соединяющей ароматические кольца, затруднено, а также в спироциклических соединениях.
Планарная хиральность[править | править код]
Плоскость хиральности присутствует в производных ферроцена, замещённых парациклофанах и др. При помощи данного термина описывают хиральное расположение внеплоскостных элементов молекулы относительно плоскости хиральности[10].
Спиральная хиральность[править | править код]
Спиральная хиральность характерна для соединений, имеющих элементы в форме спирали, пропеллера или винта, например для гелиценов[11]. Шесть ароматических колец в гексагелицене не могут уложиться в одной плоскости, поэтому образовывают спираль, которая может быть закручена влево или вправо. Данный вид хиральности наблюдается также в белках и нуклеиновых кислотах.
Топологическая хиральность[править | править код]
Топологическая хиральность связана с наличием структурной несимметричности, характерной для супрамолекул, например, катенанов, ротаксанов, молекулярных узлов[6].
Хиральность соединений со стереогенной парой электронов[править | править код]
В аминах, фосфинах, ионах сульфония, оксония, сульфоксидах хиральность может возникать из-за пространственного окружения атомов азота, фосфора, серы и кислорода. Несмотря на то, что в данных соединениях все они имеют только три заместителя, четвёртое координационное место занимает неподелённая пара электронов и происходит возникновение центра хиральности.
Хиральные амины отличаются от хиральных соединений кислорода, фосфора и серы, поскольку энантиомеры аминов, возникающие из-за стереогенного атома азота, редко могут быть разделены, так как они легко превращаются друг в друга за счёт инверсии атома азота (рассчитанная энергия активации EA для триметиламина составляет около 30 ккал/моль). В то же время соответствующие фосфины подвергаются инверсии весьма медленно (рассчитанная энергия активации EA для триметилфосфина составляет около 190 ккал/моль)[12]. Исключением из данной особенности являются амины, в которых инверсия азота невозможна, поскольку его конфигурация пространственно закреплена, как, например, в основании Трёгера.

Хиральность в неорганической химии[править | править код]
Многие комплексные соединения обладают хиральностью. Классическими в данной области являются работы А. Вернера, синтезировавшего более 40 оптически активных координационных соединений. Например, октаэдрический комплекс рутения с бипиридином [Ru(bipy)3]2+ является хиральным, поскольку три бипиридиновых лиганда в нём занимают хиральное расположение в форме пропеллера.

Связь с оптической активностью[править | править код]
Хиральные соединения и их растворы обладают способностью вращать плоскость поляризации плоскополяризованного света, что можно наблюдать при помощи поляриметра. По этой причине хиральные вещества также называют оптически активными, или оптически деятельными.
Световую волну, проходящую через раствор оптически активного вещества, можно представить в виде правой и левой циркулярно поляризованных составляющих, которые в хиральной среде распространяются с различными фазовыми скоростями, за счёт чего и возникает вращение плоскости поляризации света[13].
Хиральность в биологии[править | править код]
Многие биологически активные молекулы обладают хиральностью, причём природные аминокислоты и сахара представлены в природе преимущественно в виде одного из энантиомеров: аминокислоты, в основном, имеют l-конфигурацию, а сахара — d-конфигурацию[14].
Две энантиомерные формы одной молекулы обычно имеют различную биологическую активность. Это связано с тем, что рецепторы, ферменты, антитела и другие элементы организма также обладают хиральностью, и структурное несоответствие между этими элементами и хиральными молекулами препятствует их взаимодействию. Например, ферменты, являющиеся хиральными молекулами, часто проявляют специфическую реакционную способность по отношению к одному из энантиомеров. Подобные примеры характерны и для лекарственных соединений. Так, биологической активностью обладает лишь один энантиомер ибупрофена — (S)-(+)-ибупрофен, в то время как его оптический антипод (R)-(−)-ибупрофен в организме неактивен[15].
Гомохиральность[править | править код]
За редкими исключениями, природные хиральные аминокислоты и моносахариды представлены в виде единственного изомера из двух возможных. Так, в состав белков входят практически исключительно l-аминокислоты, а ДНК и РНК построены только на основе d-углеводов. Данное свойство химических соединений называется гомохиральностью (хиральной чистотой). Происхождение и назначение данного явления до конца не установлены, однако его часто связывают с проблемой происхождения жизни[16].
См. также[править | править код]
Примечания[править | править код]
- ↑ 1 2 IUPAC Gold Book - chirality. Дата обращения: 24 февраля 2013. Архивировано 26 февраля 2013 года.
- ↑ 1 2 Flack H. D. Louis Pasteur’s discovery of molecular chirality and spontaneous resolution in 1848, together with a complete review of his crystallographic and chemical work (англ.) // Acta Cryst. Sect. A. — 2009. — Vol. A65. — P. 371–389. — doi:10.1107/S0108767309024088. Архивировано 6 сентября 2012 года.
- ↑ Kelvin W. T. Baltimore lectures on molecular dynamics and the wave theory of light (1904). — London: C. J. Clay and sons, 1904.
- ↑ Cintas P. Tracing the Origins and Evolution of Chirality and Handedness in Chemical Language (англ.) // Angew. Chem. Int. Ed. — 2007. — Vol. 46, no. 22. — P. 4016–4024. — doi:10.1002/anie.200603714.
- ↑ Азимов А. Краткая история химии = A Short History of Chemistry / Пер. с англ. З. Е. Гельмана, под ред. А. Н. Шамина. — М.: Мир, 1983. — С. 88—89.
- ↑ 1 2 3 4 Бутин К. П. Теоретическая стереохимия. Дата обращения: 23 февраля 2013. Архивировано 29 января 2013 года.
- ↑ Потапов В. М. Стереохимия. — М.: Химия, 1988. — С. 18-20. — ISBN 5-7245-0376-X.
- ↑ IUPAC Gold Book - chirality centre. Дата обращения: 24 февраля 2013. Архивировано 26 февраля 2013 года.
- ↑ IUPAC Gold Book - axial chirality. Дата обращения: 24 февраля 2013. Архивировано из оригинала 23 декабря 2010 года.
- ↑ IUPAC Gold Book - planar chirality. Дата обращения: 24 февраля 2013. Архивировано 26 февраля 2013 года.
- ↑ IUPAC Gold Book - helicity. Дата обращения: 24 февраля 2013. Архивировано 26 февраля 2013 года.
- ↑ Kölmel С., Oehsenfeld C., Ahlrichs R. An ab initio investigation of structure and inversion barrier of triisopropylamine and related amines and phosphines (англ.) // Theor. Chim. Acta. — 1991. — Vol. 82, no. 3-4. — P. 271-284. — ISSN 1432-2234. — doi:10.1007/BF01113258.
- ↑ Трофимова Т. И. Курс физики. — М.: Высшая школа, 1990. — С. 315. — 478 с. — ISBN 5-06-001540-8.
- ↑ Овчинников Ю. А. Биоорганическая химия. — М.: Просвещение, 1987. — С. 27.
- ↑ Tracy T. S., Hall S. D. Metabolic inversion of (R)-ibuprofen. Epimerization and hydrolysis of ibuprofenyl-coenzyme A (англ.) // Drug Metab. Dispos. — 1992. — Vol. 20, no. 2. — P. 322-327. — PMID 1352228.
- ↑ Bonner W. A. Origins of Chiral Homogeneity in Nature (англ.) // Topics in Stereochemistry. — 2007. — Vol. 18. — P. 1-96. — doi:10.1002/9780470147276.ch1.